水素結合
水素結合は教科書にはないが、最も身近な水の得意な性質を決めてることや、生物にとって極めて重要な働きをしている。また、いわゆる水関連の疑似科学商法も盛んなので注意を喚起する意味もあって、すこし詳しく説明をする。
水素結合(すいそけつごう、hydrogen bond)とは、窒素、酸素、硫黄、ハロゲンなどの電気陰性度が大きな原子(陰性原子)に共有結合で結びついた水素原子が、近くの他の原子の孤立電子対の間の静電的な引力による結びつきのこと。分子間、あるいは分子内に働く結合力として、蛋白質、核酸などの生体高分子や、水、アンモニア、フッ化水素などの低分子が示す特異的な構造や機能の源となる作用である。
水の性質と水素結合
水分子は、酸素原子1個と水素原子2個が共有結合で結びついている化合物であることは、水の構造で説明した。水分子は結合に関わっている電子が酸素側に偏っていて(電気陰性度)、酸素には二つの孤立電子対があるため、孤立電子対と水素原子の間で静電気的に強い引力が働いている。
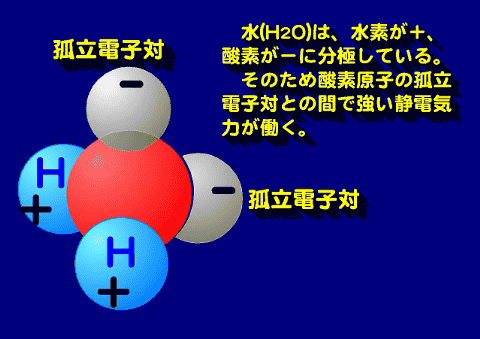
たとえば水分子では、酸素原子間の距離は2.8Å(オングストローム)で、水素原子は一方の酸素原子から約1.0Åの位置にある。この水素原子はしばしば交換される。(プロトン交換)
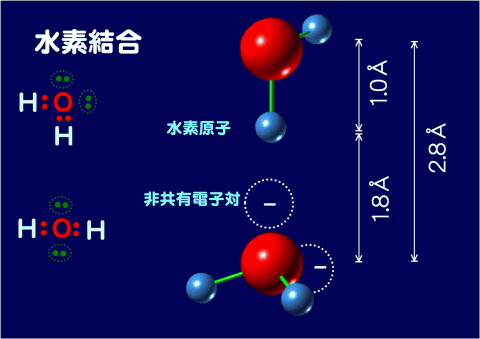
水素結合は、ファンデルワールス力よりは強く、共有結合よりは弱い。水素結合は、水の性質、たとえば相変化などの熱的性質、あるいは水と他の物質との親和性などにおいて重要な役割を担っている。たとえば水が氷になる時に体積が増えたりする現象にも水素結合が関与している。
氷は、水素結合のため図のようにとても大きな隙間を持つ固体になるため、固体のほうが液体よりも体積が大きくなる。氷が解ける、すなわち水分子の位置を固定していた結合が切れると、水分子はこの大きな隙間内に落ち込んで体積が減る。また、この水素結合による部分的な構造は液体の水においても、いくつかは残る。50℃においても半分程度は残っている。
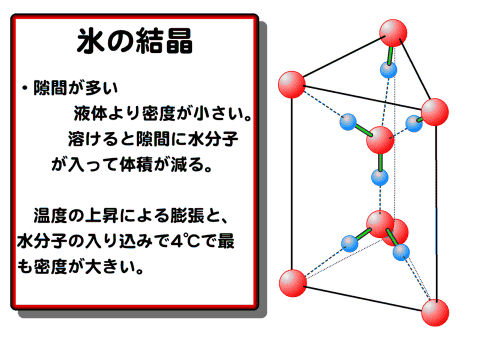
水は、その分子量(18)から想像される性質とはかけ離れた異常な物質である。
- 高い融点や沸点
- 高い表面張力
- 高い粘度
- 大きな比熱や大きな気化熱
- 4℃で最も大きな比重
- 固体(氷)になると膨張する
- 高い誘電率
- イオンの大きな溶解性を示し強力な溶媒となる。
生体における水素結合
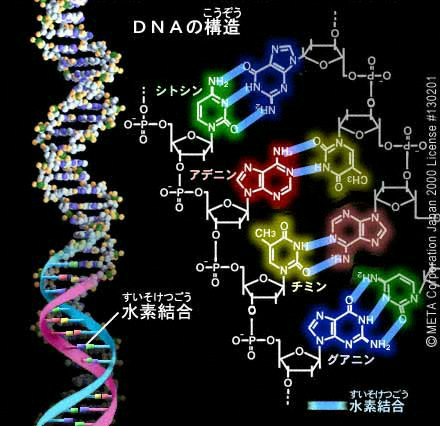 生体高分子において水素結合は、蛋白質が二次構造以上の高次構造を形成する際、あるいは核酸の中で核酸塩基同士が相補的に結びつき二重らせん構造が形成する際に必要な、重要な駆動力となっている。
生体高分子において水素結合は、蛋白質が二次構造以上の高次構造を形成する際、あるいは核酸の中で核酸塩基同士が相補的に結びつき二重らせん構造が形成する際に必要な、重要な駆動力となっている。
生体高分子において水素結合は、蛋白質が二次構造以上の高次構造を形成する際、あるいは核酸の中で核酸塩基同士が相補的に結びつき二重らせん構造が形成する際に必要な、重要な駆動力となっている。
水素結合は生物にとって非常に重要な働きをしています。人体には多量の水が含まれ、タンパク質、核酸、脂肪、炭水化物なども含まれています。これらの物質が機能するためには、水素結合が大きな役割をしているのです。これは、家は材木を組み立てて作られますが、その材木と材木をつなぎ止める役目をしているのが水素結合で言ってよいでしょう。遺伝子をはじめとするタンパク質など体内の物質を立体的な形にするために水素結合は必要なのです。
生命と水
- 分子量(18)にしては、融点も沸点も高い。
=比熱や凝縮熱・気化熱が大きい。 - 地球の温度を一定に保つ。
- 蒸気機関が可能なのは・・・
- 凍ると体積が増える。
- 氷河期に全球氷結しなかった。
- 池や海が表面が凍っても内部は液体のまま
- 強力な溶媒である。
- 塩類を溶かすことができる。
- 油は溶けない・・生命の起源に
油が水に溶けないのはなぜ?(疎水結合)
水分子どおしは、この水素結合を引き起こす極性分子であるため、液体においても強く結びついている。そのため、極性のない油などは、水分子どおしの引力を押しのけて混ざることができない。それはあたかも極性のない物質どおしが結びついているように観察されるため、疎水結合と呼ばれることがある。非極性物質はファンデルワールス力で結びついている。
配位結合
一方の原子からのみ電子が供与されている共有結合を配位結合という。アンモニアが水に溶けて生成されるアンモニウムイオンや硫酸イオンなどは配位結合。